17 Feb 2022
Proteína de bacteria que causa la brucelosis podría mejorar la inmunoterapia contra el melanoma
Así lo demostró un estudio preclínico liderado por científicos del Instituto Leloir y publicado en Scientific Reports, aunque se requieren estudios en pacientes humanos para verificar su eficacia y seguridad.
 Los autores del estudio. Arriba de izq. a der.: Fernando Goldbaum, Paula Berguer, Ariadna Soto y Ana Farias. Abajo de izq. a der.: Carla Goldin, Santiago Sosa, Camila Gil y Franz Puttur.
Los autores del estudio. Arriba de izq. a der.: Fernando Goldbaum, Paula Berguer, Ariadna Soto y Ana Farias. Abajo de izq. a der.: Carla Goldin, Santiago Sosa, Camila Gil y Franz Puttur.
Investigadores de la Fundación Instituto Leloir (FIL) comprobaron en ensayos preclínicos que una proteína de la bacteria de la brucelosis mejora la eficacia de un tratamiento contra el melanoma.
“Aunque se deben realizar más análisis para comprender completamente los mecanismos antitumorales que desencadena, la proteína lumazina sintasa (BLS) de la bacteria Brucella surge como una plataforma prometedora para la terapia contra el melanoma”, afirmó la doctora en Biología Paula Berguer, directora del trabajo e investigadora del CONICET en el Laboratorio de Inmunología y Microbiología Molecular liderado por Fernando Goldbaum en la Fundación Instituto Leloir (FIL).
Los investigadores de la FIL eligieron esa proteína porque previamente habían descubierto que tenía la capacidad de activar células del sistema inmune que tienen un rol fundamental no solo para combatir infecciones sino también tumores. A partir de este hallazgo, descrito en la revista PloS One, pensaron que podía aumentar la potencia de inmunoterapias contra el melanoma.
En la actualidad, contra distintos tipos de cáncer se administran “inhibidores de punto de control inmunológicos”, anti-PD-1 o anti-PD-L1. Este tipo de tratamientos levanta “frenos internos” del sistema inmune para destruir células tumorales.
Sin embargo, dado que la inmunoterapia con anti-PD-1 o anti-PD-L1 no genera muy buenos resultados contra melanoma, “decidimos probar una herramienta que pudiera mejorar su desempeño”, indicó Berguer.
Fácil de producir
Berguer y equipo trabajaron con BLS, una proteína proveniente de Brucella abortus pero que por ingeniería genética puede ser obtenida en grandes cantidades a partir de otra bacteria llamada Escherichia coli.
“En el laboratorio estudiamos exhaustivamente las características de BLS y observamos que, además de ser una proteína muy estable y de fácil obtención, despierta una respuesta inmunológica potente y duradera”, subrayó Berguer.
Y continuó: “Descubrimos que gran parte de la respuesta que BLS genera es gracias a su capacidad de unirse a una proteína en la membrana exterior de células de la inmunidad innata, el receptor de tipo Toll 4 (TLR4)”.
Los autores del estudio, publicado en Scientific Reports, comprobaron que en ratones con melanoma BLS tiene un efecto antitumoral per se que aumenta de manera sinérgica por el uso combinado con la inmunoterapia anti-PD-1, logrando disminuir la velocidad de crecimiento del tumor y aumentando significativamente su sobrevida.
Al estudiar qué mecanismos podrían estar actuando, los investigadores vieron que la administración de BLS en los animales portadores de melanoma hace que en las zonas cercanas al tumor disminuya la proporción de células regulatorias, que normalmente frenan la respuesta inmune y que aumenten las células capaces de montar una respuesta que ayude a eliminar las células tumorales.
Además, el tratamiento con BLS indujo un aumento en la cantidad de ciertas células inmunes llamadas “natural killers” (NK) y del interferón gamma (IFN-g), los cuales contribuyeron a generar una adecuada respuesta antitumoral en los estudios preclínicos.
“Los resultados obtenidos en nuestro trabajo sugieren que la administración de BLS incrementa la susceptibilidad del tumor al tratamiento con anticuerpos anti-PD-1. Estudios adicionales tendrían que realizarse en el futuro para poder sentar las bases para la realización de ensayos clínicos en humanos que comprueben su seguridad y eficacia”, concluyó Berguer.
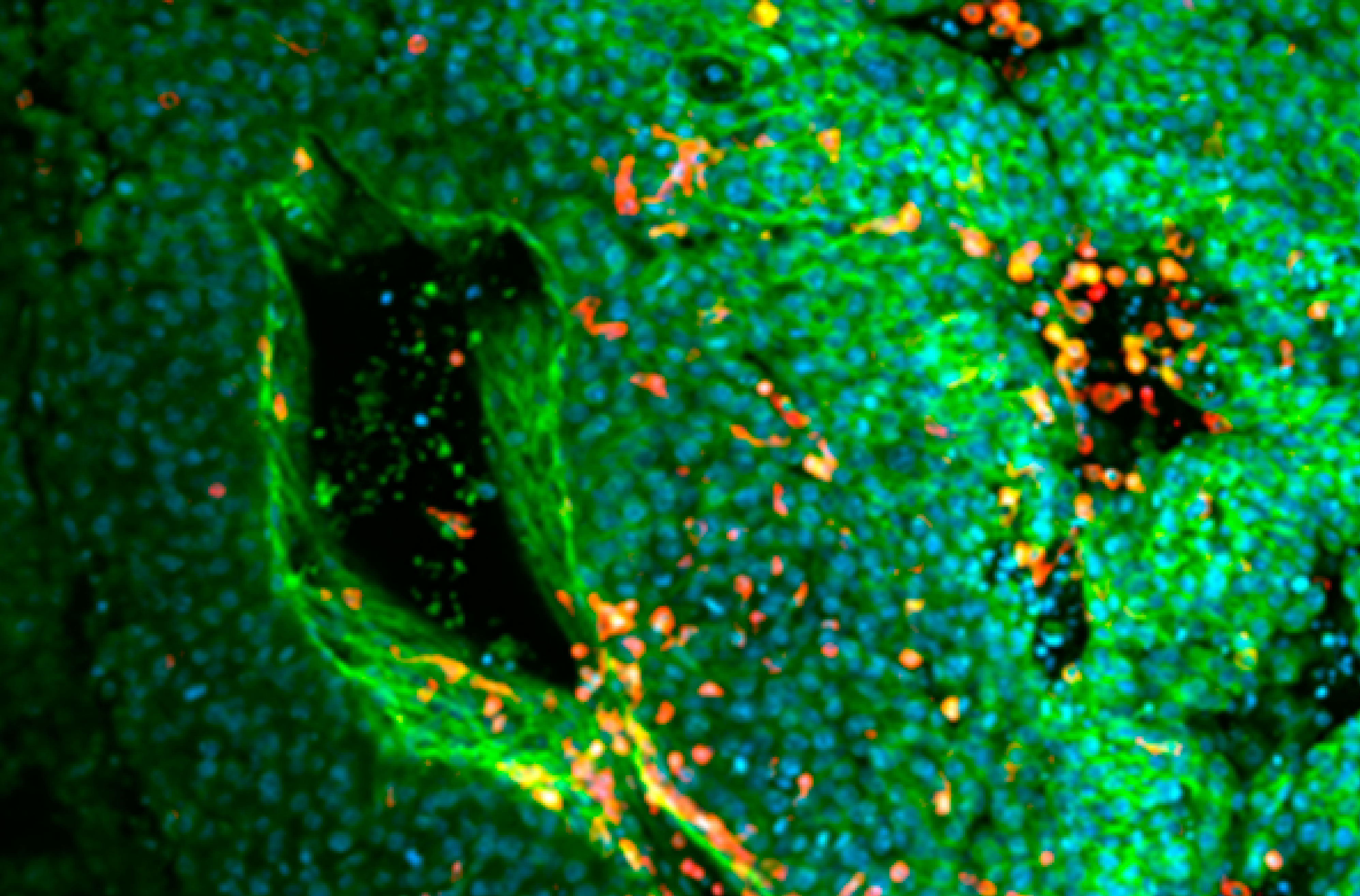
Los resultados del trabajo forman parte de la tesis doctoral de Ana Farias bajo la dirección de Berguer en la FIL. Y también participaron Fernando Goldbaum, Ariadna Soto, Carla Goldin y Santiago Sosa, de la FIL y del CONICET, y Camila Gil, de la FIL; y Franz Puttur, del Imperial College London, en Londres, Reino Unido, quien realizó un importante aporte de imágenes de microscopía de los tumores.
 Los autores del estudio. Arriba de izq. a der.: Fernando Goldbaum, Paula Berguer, Ariadna Soto y Ana Farias. Abajo de izq. a der.: Carla Goldin, Santiago Sosa, Camila Gil y Franz Puttur.
Los autores del estudio. Arriba de izq. a der.: Fernando Goldbaum, Paula Berguer, Ariadna Soto y Ana Farias. Abajo de izq. a der.: Carla Goldin, Santiago Sosa, Camila Gil y Franz Puttur.Investigadores de la Fundación Instituto Leloir (FIL) comprobaron en ensayos preclínicos que una proteína de la bacteria de la brucelosis mejora la eficacia de un tratamiento contra el melanoma.
“Aunque se deben realizar más análisis para comprender completamente los mecanismos antitumorales que desencadena, la proteína lumazina sintasa (BLS) de la bacteria Brucella surge como una plataforma prometedora para la terapia contra el melanoma”, afirmó la doctora en Biología Paula Berguer, directora del trabajo e investigadora del CONICET en el Laboratorio de Inmunología y Microbiología Molecular liderado por Fernando Goldbaum en la Fundación Instituto Leloir (FIL).
Los investigadores de la FIL eligieron esa proteína porque previamente habían descubierto que tenía la capacidad de activar células del sistema inmune que tienen un rol fundamental no solo para combatir infecciones sino también tumores. A partir de este hallazgo, descrito en la revista PloS One, pensaron que podía aumentar la potencia de inmunoterapias contra el melanoma.
En la actualidad, contra distintos tipos de cáncer se administran “inhibidores de punto de control inmunológicos”, anti-PD-1 o anti-PD-L1. Este tipo de tratamientos levanta “frenos internos” del sistema inmune para destruir células tumorales.
Sin embargo, dado que la inmunoterapia con anti-PD-1 o anti-PD-L1 no genera muy buenos resultados contra melanoma, “decidimos probar una herramienta que pudiera mejorar su desempeño”, indicó Berguer.
Fácil de producir
Berguer y equipo trabajaron con BLS, una proteína proveniente de Brucella abortus pero que por ingeniería genética puede ser obtenida en grandes cantidades a partir de otra bacteria llamada Escherichia coli.
“En el laboratorio estudiamos exhaustivamente las características de BLS y observamos que, además de ser una proteína muy estable y de fácil obtención, despierta una respuesta inmunológica potente y duradera”, subrayó Berguer.
Y continuó: “Descubrimos que gran parte de la respuesta que BLS genera es gracias a su capacidad de unirse a una proteína en la membrana exterior de células de la inmunidad innata, el receptor de tipo Toll 4 (TLR4)”.
Los autores del estudio, publicado en Scientific Reports, comprobaron que en ratones con melanoma BLS tiene un efecto antitumoral per se que aumenta de manera sinérgica por el uso combinado con la inmunoterapia anti-PD-1, logrando disminuir la velocidad de crecimiento del tumor y aumentando significativamente su sobrevida.
Al estudiar qué mecanismos podrían estar actuando, los investigadores vieron que la administración de BLS en los animales portadores de melanoma hace que en las zonas cercanas al tumor disminuya la proporción de células regulatorias, que normalmente frenan la respuesta inmune y que aumenten las células capaces de montar una respuesta que ayude a eliminar las células tumorales.
Además, el tratamiento con BLS indujo un aumento en la cantidad de ciertas células inmunes llamadas “natural killers” (NK) y del interferón gamma (IFN-g), los cuales contribuyeron a generar una adecuada respuesta antitumoral en los estudios preclínicos.
“Los resultados obtenidos en nuestro trabajo sugieren que la administración de BLS incrementa la susceptibilidad del tumor al tratamiento con anticuerpos anti-PD-1. Estudios adicionales tendrían que realizarse en el futuro para poder sentar las bases para la realización de ensayos clínicos en humanos que comprueben su seguridad y eficacia”, concluyó Berguer.
Los resultados del trabajo forman parte de la tesis doctoral de Ana Farias bajo la dirección de Berguer en la FIL. Y también participaron Fernando Goldbaum, Ariadna Soto, Carla Goldin y Santiago Sosa, de la FIL y del CONICET, y Camila Gil, de la FIL; y Franz Puttur, del Imperial College London, en Londres, Reino Unido, quien realizó un importante aporte de imágenes de microscopía de los tumores.